����һ��������Ѫ֬�쳣
����2�������������ӷ�����Ѫ�ܲ���֢��Σ�գ��������ҵ��̴������ƻ���NCEP����������������α��棨ATP��������Ϊ���IJ���Σ֢������������10���ڷ������IJ��ľ���Σ���Ըߣ���10���ڷ������IJ��¼��İٷֱȡ�20%�����������߹��IJ�Σ���Ըߵ�ԭ���Ƕ��ģ�������Ѫ�ǡ���Ѫѹ��Ѫ֬�쳣�����̡�����״̬����֢���ӵIJ���ȡ���ˣ�����������������Ѫ�Ǻ�Ѫѹ�⣬��Ӧ���Ӷ���Ѫ֬�쳣���ڵ��������IJ�Σ�����ؽ��п��ơ�
��������������Ѫ֬�쳣�ı���
����1.1��������û�����ƻ������Ƶ�����£�������Ϊ����������TG�����ߣ����ܶ�֬�����̴� ��HDL-C�����ͣ��ܵ��̴���TC���͵��ܶ�֬�����̴���LDL-C��ˮƽҲ�����������ȵ���ǿ�����ƣ�����Ѫ֬��֬����ˮƽ�ɵ�����ͬ������Ա�ķ�������Ⱥˮƽ�����⣬��Ѫ�ǿ��Ʋ���ʱLDL-C�����ǻ�����������֬���ף�a��[Lp��a��]ˮƽ���������ߣ��б�����������������˥�ߡ������������ʱLp��a��ˮƽҲ���ߡ�
����2.��2������Ѫ֬�쳣�ϳ��������ͱ���ΪTG���ߣ�HDL-C���ͣ�LDL-Cͨ�����������Ⱥ�����Բ��졣С����LDL-C���ǻ���������LDL-C���ӣ��������Ӳ���һ������LDL-C��ˮƽ�����ӡ������о���Ϊ����2������Lp��a��ˮƽ�����ӡ�
����3.�����ߵ�Ѫ֬�쳣Ҳ���ɼ̷����ػ�ϲ��м̷��������£�����Ϻ�����ʱӦ��ע�⡣�����ļ̷����ذ�����״�ٹ��ܼ���֢�������ۺ���������������˥�ߡ������Ըβ���ҩ���������������������������ͼ�����Ƥ�ʼ��صȣ���һЩ���ص�Ѫ֬�쳣����Ҳ���ܺϲ��м����Ŵ���֬��л������
��������������Ѫ֬����Ŀ��
����������̫����2������������2002���ƶ���Ѫ֬����Ŀ�꣨�����棩���14-1��
����
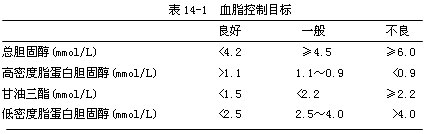 ��
������LDL-C�ǵ��¹��IJ�����ҪΣ�����أ�����LDL-C���ٴ����飨4S��CARE*��Ҳ֤��������LDL-C���������������߹����¼��ķ����ʣ���Ч�����ڻ���ڷ�������Ⱥ��LDL-C�Ŀ���Ŀ��Ӧ��ͬ���ѻ����IJ�����Ⱥ����LDL-C<2.5mmol/L.����LDL-CռTC60%��70%����LDL-C�Ľ��ͣ�TCҲ�ɽ���Ŀ��ˮƽ��
������HDL-Cˮƽ����IJ������ʳʷ��ȣ�HDL-C�������߷������IJ�ǿ������Ԥ�����أ����HDL-CˮƽӦ>1.1 mmol/L����������һЩ�о��ͷ���������TG�ǹ��IJ��Ķ���Σ�����أ�����Ҫ����ΪijЩ��������������֬���ף�TGRL�������¶�������Ӳ���ԣ����⣬��TG���ϲ��е�HDL-C������Ѫ֬�쳣�ʹ�л�ۺ�����TGӦ������<1.5 mmol/L��
����*4S=˹������ά��������͡�������飻CARE=���̴������¼�����
����������Ѫ֬�쳣������
����Ѫ֬�쳣�Ĺ�����������ʳ���ڡ��˶����������ء�����Ѫ�Ǻ�ʹ�ý�֬ҩ��ȡ�
����1.��ʳ���ں��˶��ǵ�֬���ƵĻ�����ͨ����ʳ���ں��˶����ɽ������ء�TG������HDL-C������ȵĽ���LDL-C�����á���̫����2������������2002���ƶ���Ӫ��ԭ����Ҫ���ݣ������棩���14-2��
14-2Ӫ��ԭ����Ҫ����
| Ӫ���� | ���� |
| ֬�������� | ռ��ʳ���ȿ�25%��30% |
| ����֬���� | ռ֬��������<1/3 |
| ƽ�ⵥ������֬����Ͷ����֬���� | ռ��ʳ���ȿ�55%��65% |
| ����̼ˮ������ | ռ��ʳ���ȿ���15% |
| ����̼ˮ������ | �ﵽ�ͱ����������� |
�������Դ�л�ۺ���Ϊ��Ҫ���ֵķ��֡���TG��HDL-C���͵�2�������ߣ���Ҫͨ���������أ��������ȿ��������˶������ʵ�����̼ˮ�����̼ˮ������ռ���ȿ���50%�������ߵ�̼ˮ����������ȿ���60%��������HDL-C���ͺ�TG���ߡ���������ͨ��Ӫ��ʦ�õ�������ʳָ����Ҫ���̺ͼ������ƣ��ı䲻�������ʽ��
����2.����û�в���֢��1������ͨ��ʹ���ȵ��أ��ϸ����Ѫ�ǣ�������ȫ����Ѫ֬�쳣����2�����������Ѫ�ǿ��ƿɽ���TG��HDL-Cˮƽû�б仯��������ߣ�LDL-Cˮƽ������ȵĽ��͡�
����3.���õ�֬ҩ�
����1�� ��͡��ҩ���͡��ҩ��Ϊ�Ǽ��������øA��HMG-COA����ԭø���Ƽ�����ҩ��Ҫ����LDL-C��TC������һ���̶ȵĽ���TG���ã���������Ҫ�ϸ�������͡��ҩ��һ�����������˯ǰ���ã��������нϺõ������ԣ�����Ҫ�������Ǹ�ø���ߺͼ����������ڻ�Ժ����Ըβ����ߡ�
����2�� ��������֬����Ҫ���ڽ���LDL-C��TC��ҩ�����Ҫ�����ð���θ����֢״�Լ�����ijЩͬʱ����ҩ������ա���ҩ�����ڼ������쳣��-֬����Ѫ֢������������TG����������TG>4.5mmol/L�Ļ��ߣ�TG>2.3mmol/L����Խ��ɡ�
����3�� ������������������ɽ���TG��LDL-C��Lp��a����ͬʱ������HDL-C��Ҳ�ɽ�СLDLת���������СLDL����Ҫ�������Ǹζ��ԡ�������Ѫ֢�Լ�Ѫ�����ߡ�һ����Ϊ2��������Ӧ����ʹ�ô�������ᣨ3g/d�����ɿ�����С�������ᣨ<2g/d������������������Ըβ�������ʹ�综�ߡ����������ﰢ��Ī˾�����ý��ᣬ������2������
����4�� ��ά����������������֬ҩ����ҪΪ����TG������HDL-C������һ���̶Ƚ���LDL-C���á�����ҩ����нϺõ������ԺͰ�ȫ�ԣ���Ҫ��������θ����֢״����ʯ֢�������а鼡�ἤø���ߵļ������������������ظ����Ļ��ߣ�������������������Ҫ���û����ʹ�á�
����5�� ������֬ҩ�n-3֬����[�����ᡢ��ʮ̼��ϩ�ᣨEPA������ʮ��̼��ϩ�ᣨDHA��]�ڽϴ����ʱ�ɽ���TG�������Ƹ�TGѪ֢ʱ����Ϊһ��ѡ��Ŀǰ�о���Ϊ�Ƽ�������Ʒ����Ƽ�����Ԥ�����IJ�ΪĿ�ĵ����ơ�
����4.��֬���Ƶ�ѡ��
����1�� ��LDL-C�����ƣ���������Э�ᣨADA��������������ߺϲ��й��IJ����Ѫ�ܼ�������LDL-C��2.6mmol/Lʱ������ʳ���˶������ʽ������ͬʱ��ʼҩ�����ƣ���������й��IJ����Ѫ�ܼ�����LDL-C��3.35mmol/Lʱ����ʼ��ʳ���˶��Լ�ҩ�����ƣ���LDL-C��2.6��3.35mmol/L֮��ʱ�����ȿ�����ʳ���˶����ƣ���Ч��������ʱ�ټ���ҩ�����ơ�����Ѫ�Ǻ͵�֬����Ӧͬʱ���У�ҩ��������ѡ��͡�࣬��ѡ��������֬���ŵ���أ��нϺõĽ���LDL-C���ã��ر��ʺϻ���Ը�֬Ѫ֢������LDL-C�ϸߣ�����δ���ʱ���ɿ��ǼӴ���͡��ҩ��ļ�����������ҩ������͡��ҩ���뵨������֬���õȡ�
����2�� ��TG�����ƣ����ȸı����ʽ���������ء��������ƺ��ϸ����Ѫ�ǣ��Խ���TG�dz���Ч����Ѫ���Ѿ����ܵõ����ƺɿ���ҩ�����ƣ���ѡ��TG��2.3��4.5mmol/Lʱ��ʼҩ�����ơ���ѡ��ά����ҩ���͡�������Ƹ�TG���LDL-Cʱ��һ����Ч��
����3�� ����Ը�֬Ѫ֢����LDL-C��TG�������ƣ��ڿ���Ѫ�ǵ�ͬʱ�ɿ�������͡��ҩ��ϸ�������͡��ҩ�����Ч����TGˮƽ����LDL-C�Ѵ�꣬TG��2.3mmol/L�ɿ����滻Ϊ��ά���������͡����ã����ֺ��û����Ӽ�����Σ�գ�Ӧ�ر����ʹ�á���ijЩ����£�TG>5.6mmol/L������Ŀ��������ͨ������TG����ֹ���������ף�ֻ�е�TG<5.6mmol/Lʱ�����ܽ�ע���������ڽ���LDL-C�ϡ�
����4�� ��HDL-CѪ֢�����ƣ����ܼ������ء��˶������̺Ϳ���Ѫ�Ƕ����HDL-C��Ч���������������Ҫҩ�����ơ�������ҩ������Ч����HDL-C����Ӧ����ʹ�ã������ѡ����ά�������
�������ģ�����顢��ü�����ַ�ҩ
��������������ÿ����Ѫ֬һ�Σ��������ݰ���TC��TG��HDL-C��LDL-C���ɹ�ʽ�����ֱ�Ӳⶨ��������Ѫ֬��飬���ȿ�ʼ��ʳ���˶��ȷǵ�֬ҩ�����ƣ���3���º�Ѫ֬ˮƽ���ﵽĿ���������ƣ���ÿ6��12���¸���һ�Σ��翪ʼҩ�����ƣ�һ���״��������ҩ��6��8�ܣ�����ܴﵽ����Ŀ�꣬�ɸ�Ϊÿ4��6���¸���һ�λ������ÿ��һ�Σ����翪ʼ���ƺ�δ��Ŀ�꣬������Ҫ���Ӽ�����������ҩ��ҩ����ÿ6��8�����һ�Σ�ֱ���ﵽĿ������ÿ4��6���¸���һ�λ������������ݰ������۵�֬Ч�������á���������ڻ���ַ�ҩ������ַ�ҩ�Ǽ��ٹ��IJ�Σ���Ե���Ҫ��ʩ��
���������������Ѫѹ
��������Ѫѹ�����ϲ����ڣ�����Ѫ��ϵͳ�м�ǿ��Σ���ԡ�1�������ڲ������������ָ�Ѫѹ��2�����������ϲ�ԭ���Ը�Ѫѹ��������2��������֮ǰ��ͬʱ��֮����֡������ϲ���Ѫѹ��Ⱥ������Ѫ��Σ�����������л����ĸ�Ԥ�����ƣ���Ԥ������Ѫ�ܺ�Ѫ�ܲ���֢��Ԥ����Ѫ���¼��ķ�������������������ӳ�������������ʮ����Ҫ�����塣
�����������ݲ��ʺ��ڻ�����Ѫѹ�����ﻼ�ߡ�
������һ����Ѫ��ϵͳΣ��
������Ѫѹ�����ϲ����ڶ���Ѫ�ܵ�Σ���г˻�ЧӦ����Ѫѹ��ʹ�����ߵ���Ѫ�ܷ�����߽�2������˶��߲������Ѫ��Σ���ľ�ЧӦ����ͨ��Ⱥ��4��8����ͬ���أ�����Ҳ��ʹ��Ѫѹ��Ⱥ����Ѫ�ܷ�������2�����������Ⱥ�У������ָ�Ѫѹ��������ʱ����������Ӳ���Ļ��������ӣ�����Ѫ�ܼ����ĸ��ʹ��ƿɸߴ�50%�����й��IJ��ɸߴ�25%����Ѫ�ܼ��������ķ���Ҳ�������ߡ�
���������ҹ�1999���ƶ��ĸ�Ѫѹ����ָ�ϣ����ϲ���Ѫѹ��Σ���൱�ڸ�Ѫѹ�ϲ�����Σ�����ء����ϲ����ĸ�Ѫѹ��Σ���ֲ���ڡ���Σ��֮�ϣ����������������ж��Σ�����أ��������ۡ���������Ѫ�ܲ���֢���Ѫѹ���ص�����ˣ����߲����Σ�շֲ㳣���ܴﵽ���ܸ�Σ��ˮƽ����14-3��14-4����
������ѪѹҲ������������Ѫ�ܲ������ҪΣ�����أ������ÿ��ܸ����ڸ�Ѫ�ǣ�Ӣ������ǰհ���о�UKPDS�Ľ����ʾ������Ѫѹ���Լ���Ѫ�ܲ���֢����37%��������Ѫ��ֻ����25%��
����ֵ��ע����ǣ���Щ֤����ʾ��Ѫѹ������������Ѫ�ܲ���Ĺ�ϵ���ڸ�Ѫ�ǣ�����������Ѫ�ܼ����Ĺ�ϵ���ڸ�Ѫѹ��
|
����Σ�����غͲ�ʷ |
1�� |
�� |
2�� |
�� |
3�� |
|
* SBP140��159 �� DBP90��99 |
* SBP160��179 �� DBP100��109 |
* SBP��180 �� DBP��110 | |||
|
I������������ |
��Σ |
��Σ |
��Σ | ||
|
II1��2�������� |
��Σ |
��Σ |
�ܸ�Σ | ||
|
III��3��Σ�����ػ������������ |
��Σ |
��Σ |
�ܸ�Σ | ||
|
IV�����ٴ���� |
�ܸ�Σ |
�ܸ�Σ |
�ܸ�Σ | ||
����*SBP=����ѹ��DBP=����ѹ
��14-4 Ӱ���Ѫѹ����Ԥ���Σ�����ؼ��䶨��
|
��Ѫ�ܼ���Σ������ |
�������� |
�����ٴ���� |
| 1������Σ�����طֲ��Σ������ | �����ҷʺ��ĵ�ͼ�������Ķ�ͼ��X�ߣ� | ��Ѫ�ܲ� |
| ����ѹ������ѹˮƽ��1��3���� | �� | ȱѪ������ |
| ����>55�� | �ͣ���Ѫ����Ũ���� | �Գ�Ѫ |
| Ů��>65�� | �����ߣ�106��177��mmol/L ��1.2��2.0mg/dl�� | ��������ȱѪ���� |
| ���� | �� | ��TIA�� |
| �ܵ��̴���5.72mmol/L��220mg/dl�� | ������X��֤ʵ�ж������� | ���༲�� |
| ���� | �߿飨���������Ķ������ɶ������������� | �ļ����� |
| ������������<55�꣬Ů<65�꣩ ������������<55�꣬Ů<65�꣩ | ����Ĥ�ձ�����Զ�����խ | �Ľ�ʹ����״����Ѫ���ؽ�������Ѫ������˥�� |
| 2������Ԥ�������Σ������ | �� | ���༲�� |
| HDL-C���� | �� | �������� |
| LDL-C���� | �� | ������˥�ߣ�Ѫ����Ũ��>177��mmol/L��2.0mg/dl �� |
| ������������ | �� | Ѫ�ܼ��� |
| �������������� | �� | �в㶯���� |
| ���� | �� | �ضȸ�Ѫѹ������Ĥ���� |
| ��������ٵ����ʽ | �� | ��Ѫ������ |
| Ѫ����ά����ԭ���� | �� | ����ͷˮ�� |
���������������ɸ��
����������ɸ���ͬʱ����Ѫѹ��Ѫѹ���������Ϊ�����ճ����ﲻ��ȱ�ٵ����ݣ���ҪʱҪ���в�ͬ��λ�IJ������Է������������Ѫѹ��Ӱ�졣
����������������ѹ��130 mmHg�ͣ�����ѹ��80 mmHg��Ӧ��������ظ���������֤ʵѪѹ�Ƿ����ߡ�
�������ڸ�Ѫѹ��Ѫѹ��140/90 mmHg����Ⱥ����������Ӧ������Ѫ�ǻ�ͺ�Ѫ�ǵļ�⣬���ڻ���������Σ����������֡�������ʷ�������40���ߣ��������Ѫ�Ǽ�⡣
����Ѫѹ�IJ�����Ѫ�ǵļ��Ӧ���ﵽһ����Ƶ�ȣ��Լ�ʱ���������ϲ����ڡ���������Ӧ��ÿ3���²���һ��Ѫѹ����Ѫѹ���ߺͽ��ܽ�ѹ�����ߣ��˹��������Բ�Ѫѹ������Ѫѹ���Ƶ�ȣ�����ÿ�ܲ���һ�Ρ�
��������������
����1.����Ŀ��
����1����������Ѫ�ܺ�Ѫ�ܲ���֢�ķ�����
����2���������ܸ�Ѫѹ���˵İ����١�
����3�������������²��ʣ�����ߵ������������ӳ�������
����2.����Ŀ���Ѫѹ���
����1��һ�����Ŀ��ΪѪѹ��130/80 mmHg
����2����������Ӧ��140/90 mmHg
����3����24Сʱ����ס�1g��ѪѹӦ��125/75 mmHg
����4��ҩ������24Сʱ�ڵĹȷ��Ӧ��50%��
����5��������Ӧ����Ѫѹ��130/80 mmHgʱ��ʼ��Ԥ��
����6����ʼ���ƺ�Ӧ���м��Ѫѹ�����������ȷ�����ƴ�ꡣ
����3.��ҩ������
������ҩ��������ָ����Ϊ�����ʽ���Ż���Ӧ����Ϊ����Ѫѹ���ƵĻ���������Ѫѹ���ߵĸ�Ԥ��ʩ����Ѫѹ����130��139/80��89 mmHgˮƽʱ�����Ž��з�ҩ���Ԥ������3���£�����Ч��ʼҩ�����ơ���ҩ���Ԥ������
����1�����̣��ճ�����Ӧ���������л��߽��̣������������ѯ����Ҫʱ����ҩ����̡�
����2�����أ�����10%���������ټ���5kg
����3���������ƣ�����ÿ���Ҵ�����Ӧ��20��30g��Ů�ԡ�10��20g��
����4���������Σ�ÿ���Ȼ��ơ�6g��
����5���Ż���ʳ�ṹ�����ˮ�����߲ˣ�����֬�����롣û����ȷ��֤��֤�������Ĵ�ʩ�粹����Ӫ���أ����Ӹơ�þ����ά�ػ�������Ч��
����6����ǿ���������첽������Ӿ��ÿ��5�Σ�ÿ��30���ӡ�
����7����������ѹ���������ֹ���̬��
����4.ҩ������ԭ��
����1������С������ҩ���ƣ�����Ч��ȡ������ҩ��һ�㲻���ų����������
����2���ڿ��ƴ���ͬʱ����˰����ٱ����ͶԲ���֢���洦��
����3������ҩ�︱���ã�������١���л�IJ���Ӱ�졣
����5.��ѹҩ�����Ӧ֢�ͽ���֢����14-5��
����6.������ҩ
����������ҩ���Լ��ٵ�ҩ�Ӵ���������ĸ����ã�����Эͬ������ǿ��Ч���֮����������ã����������ۺϱ������ã��ڶ�������Ԥ����������ҩ�����DZ�Ȼ���ơ�Ŀǰ���Ƽ���������ҩ����������
����1��Ѫ�ܽ�����ת��ø���Ƽ���ACEI����Ѫ�ܽ�����II�������ͼ���ARB���������
����2����ͨ�����ͼ���CCB������������ͼ���
����3��ACEI��CCB��
����4�����������������ͼ���
����5���Ƽ������������ʵĸ����Ƽ�����С����ACEI��С�������������������Ƽ��ܶ࣬�ٴ���Ч�϶���
��14-5 ��ѹҩ�����Ӧ֢������֢��������
|
ҩ������ |
��Ӧ֢ |
����֢ |
������ |
|
����� |
����˥�� | �����ڸ�Ѫѹ | �����Ǻ�Ѫ֬�쳣 |
| ������ | �� | ���� | |
| �����ڸ�Ѫѹ | �� | ��������� | |
|
���������ͼ� |
�Ľ�ʹ | ����������� | Ѫ֬�쳣 |
| �ļ������� | �Ķ����������� | ����Ѫ�ܹ�Ѫ���� | |
|
CCB |
�Ľ�ʹ | ���ഫ������ | ��֫ˮ�� |
| ������ | ��ά������ض����� | �ض���˥ | |
| �����ڸ�Ѫѹ | ����˥�� | ��ά������ض����� | |
| ����Ѫ�ܼ��� | �� | �� | |
|
ACEI |
����˥�� | ���� | �ɿ� |
| �����ҹ��ܲ�ȫ | ˫����������խ | ��������� | |
| �ļ������� | ��Ѫ�� | �� | |
| �������� | �� | �� | |
|
ARB |
��ACEI�п��Է�Ӧ���� ͬACEI | ͬACEI | �� |
|
���������ͼ� |
ǰ���ٷʴ� | ˫����������խ | ֱ���Ե�Ѫѹ |
| ����˥�� | ˫����������խ | �� |
����������������IJ�
�������IJ���CHD����������Ҫ��Ѫ�ܺϲ�֢���߱���������CHD�߸ߴ�72.3%,Լ50%��2�������������ʱ����CHD�������������ּ���CHD�ķ�չ��2001���������ҳ��˵��̴������ƻ������α��棨ATP����ȷ����������ǹ��IJ���Σ֢�����л�ҽѧ������ѧ�ֻ�2001����֯�Ծ���������4����10��ҽԺסԺ�����߲���֢�����ʵ��飬�ϲ�������Ѫ�ܲ���֢�߸ߴ�93%�����и�Ѫѹռ41.8%, CHDռ25.1%,��Ѫ�ܲ�ռ17.3%,Լ80%��������������Ѫ�ܲ���֢������75%����CHD��Ϊ������2��4������˴�ij�������Ͻ������ķ��Σ���ʼ��������ҪĿ�ľ��Ǿ����ܵ�Ԥ�����ӻ�CHD�ķ������Ӷ���������CHD������.
�������IJ�ͨ��ָ���ڹ�״��������Ӳ���߿켰���߿����ѳ�Ѫ��Ѫ˨�γ�,�����ļ�ȱѪ�뻵���ļ���.���IJ��������ٴ�������:1�������ȶ����Ľ�ʹ��stable angina pectoris,SAP��;2�����Թ�״�����ۺ�����acute coronary syndrome,ACS��,�������ȶ����Ľ�ʹ��unstable angina,UA������ST��̧���ļ�������non-ST-segment elevation myocardial infarction,NSTEMI����3��ST��̧���ļ�������ST-segment elevation myocardial infarction,STEMI�������ļ�������acute myocardial infarction,AMI�������������IJ�ʱ�����ı�����أ����ٴ����֡�������Ԥ����������߲�����ͬ��
������һ�� �����ȶ����Ľ�ʹ
�����Ľ�ʹ��һ�����ء���������β�����Ϊ�������ۺ��������ͱ���Ϊ��1���ز����ʳ�Ϊ��ʹ��������ѹ�Ȼ���ظУ����ǵ���������ʹ��2����λ���عǺɷ��䵽�����ϸ������ۣ�3������ʱ�伸���ӣ�4�����ۻ�����������Ϊ����5����Ϣ�����º����������Ƭ����30�����������ڻ��⡣�������Ľ�ʹ�������͡�
�����Ľ�ʹͨ�������ڹ�״������1֧�Ĵ�������۵Ļ��ߣ�����ʱ�ĵ�ͼ��Ӧ��������ȱѪ�Ըı䡣Ȼ���Ľ�ʹ��ɷ������������ಡ���Ĥ�����ļ��ʺ������ಡ�ȣ���ɼ��ڹ�״�������λ�Ѫ����Ƥ���������йص��ļ�ȱѪ����ʱʳ�ܡ��رڻ�β��ȷ���Ѫ�ܼ�����������Ľ�ʹ������Ϲ�״��������Ӳ�������ಡ�Ľ�ʹʱӦ����𡣣���14-6��
��14-6 ��ʹ���ٴ�����
|
���� |
֢״ |
| �����Ľ�ʹ����ȷ�ģ� | 1.���ʺͳ���ʱ����͵��عǺ��ʸУ� |
| 2.���ۺ������������շ��� | |
| 3.��Ϣ���������Ƭ����Ի��� | |
| �ǵ����Ľ�ʹ�����ɣ� | �������������е����� |
| ����Դ����ʹ | �������������е�һ��߱��������� |
����2������֢״���ļ�ȱѪ�������������������
��������Ҫ�㣺1������֢ʱ����˾ƥ��75��300mg/d���併�������������ʵ�Ч�����������д��ڷ������ߡ�
����1������֢ʱ���������ļ�������Ӧ�æ��������ͼ����乣��������������ߴ��ڷ������ߡ�����ע����������ͼ������ڸǵ�Ѫ�Ƿ�Ӧ������������
����2�������������������ܲ�ȫ����Ӧ��Ѫ�ܽ�����ת��ø���Ƽ���ACEI����
����3����ȷ�������Ϊ���IJ�����LDL-C>120mg/dl��3.1mmol/L���Ļ��߿��õ�֬ҩ�����Ǽ��������øA��HMG-CoA����ԭø���Ƽ�����LDL-C��<100mg/dl��2.6mmol/L����
����4�����º����������Ƭ��ʹ��������������������Ľ�ʹ�����¾����ļ�����������֢ʱ���æ��������ͼ������Ľ�ʹ��
����5�������������ͼ��н���֢ʱ�����ó�Ч����������ͨ�����ͼ���Ч�������Ƽ���
����6�����ϲ����IJ����߹�״������Ӱ������Ϊ���������Բ��䣬��2֧�������ǰ��֧���˲����3֧������ѡ�ù�����������CABG������Ϊ���Ľ�ʹ����֧�������ҹ���������Ҳ��ҩ�����ƻ�����Ƥ����Ѫ�ܳ�������PTCA����֧��ֲ�롣
����7������ǿ�����ƿո�Ѫ�ǡ��ͺ�Ѫ�Ǽ��ǻ�Ѫ�쵰�ף�HbA1c���ﵽĿ��ֵ��
�������������Թ�״�����ۺ���
�������Թ�״�����ۺ�����������ȱѪ����ʹ�����ĵ�ͼ���Ա���ΪST��̧����û��ST��̧�ߡ������ST��̧�ߵĻ������շ���Q���ļ�������QMI���������������Է�Q���ļ�������NQMI����û��ST��̧�ߵĻ��߷������ȶ����Ľ�ʹ��UA����NQMI��������֮��ļ�������ȡ����ѪҺ���Ƿ���Լ���������[���Ƶ���T��I��TnT��TnI������⼡�ἤø��CK-MB��]�����Թ����ۺ�����ָ�����ļ�ȱѪ�����һ���ٴ�֢״������ͼ����
����
 ��
���������Թ�״�����ۺ����ķ���������ȶ����Ľ�ʹ����Q���ļ�������Q���ļ�����������̸ֻ���ȶ����Ľ�ʹ����Q���ļ�������Q���ļ��������������ļ�������Ϻ�����ָ�ϡ�
���������߷������Թ�״�����ۺ����Ϸ������߲��۶��ڼ����������ʾ�����ʽϸߣ�Ԥ������ء�
�������Թ�״�����ۺ�������Ҫ�㣺
����1������Σ�շֲ㡣���й��IJ������ļ�ȱѪ��ǰ�����ʵĻ��߶�Ӧ������Σ�շֲ������������Ľ�ʹ֢״��������12�����ĵ�ͼ���ļ����˵�����������TnT��TnI��CK-MB�쵰�ס�����C��Ӧ���ף�hsCRP����������ָ֢�꣬�����з������Թ�״�����ۺ����Ļ��������䷢��������������������ȱѪ�¼���Σ�ճ̶ȣ��ɷֵ�Σ����Σ����Σ����Σָ��Ϣʹ��ҹ��ʹ���ĵ�ͼ�������ޱ仯����Σ����ָ�з�ˮ�ף�������ʹ>20���ӣ��Ľ�ʹ���б����ɡ��ε׆������³��ֶ���귴����������ԭ�������ı䣬��Ѫѹ��ST�ζ�̬�ı��1mV���ǵ�Σ���Ǹ�Σ����������Σ�����Ľ�ʹѸ�ټӾ硢ԭ���ļ�������TnT���ߡ�hsCRP���������߳���ʾԤ��ϲ��������ʹ֢״�������ԣ�������֢״���������ı����أ���������Σ���Σ���ߡ�
����2���϶�Ϊ���Թ�״�����ۺ������߲��н������ز����ʡ��ļ����˱�������Լ��³���T�����á�Ѫ������ѧ�쳣���ĵ�ͼ�������������輱��סԺ������
������ �����ļ�ȱѪ���ƣ����º��������������������������ע����Ѹ�ٻ���ȱѪ�����֢״������礻���������������������������ز���������֢ʱ�ɾ�����ע���������ͼ�Ȼ��ڷ��������������������ϰ����˼�ACEI��
������ ѪС���뿹�����ƣ�Ѹ�ٿ�ʼ��ѪС�����ƣ���ѡ��˾ƥ�ּ��̽���������Ӧ�ã���˾ƥ�ֹ�����θ�����������������߿����������ף������߿�ѪС�����ƽϷ������߽��������ʽ϶ࣻ����ҩ���ѡ��ͨ���ء��ͷ��Ӹ��أ�LMWH����LMWH������ͨ���أ�ѪС���ǵ�������������GpIIb/IIIa������������Ч��������������ơ�
������ ��Ƥ����Ѫ�ܳ�������PTCA����������������CABG����ѡ�������߶�����Σ����״������Ϊ�����Բ��䣬2֧��3֧����������ѡCABG����Ϊ2֧�����������ǰ��֧���˲������д�Ƭ����ļ�Ҳ��ѡPTCA��
������ ��Ժ���������ȶ����Ľ�ʹ�ͷ�ST��̧���ļ����������ڳ���2��3���º��չΪ�ļ��������������ļ�����������Σ�սϴ����ں�1��3���¶��������ٴ������������ȶ����Ľ�ʹ���ơ�Ҫ�Ի��߽��н���������ѵ�������ҩ�����Ƽ���á���Ӧǿ���������ϸ���ơ�
����������ST��̧���ļ�������STEMI��QMI��
�������ҹ������ļ�������Ϻ�����ָ�ϡ���Ӧǿ�������ļ���������˨��Ӧ֢ʱ�����߽Ϸ������ߵ�������������״�PTCA�ɹ���������������ƣ�������խ�ʼ�����Ԥ��Ϸ������߲2֧��3֧��״�����������ѡ��CABG����˾ƥ�֡����������ͼ���ACEI��Ӧ�þ��Ϸ������ߵ����
�����ġ����ϲ���Ѫ�ܲ�
������Ѫ�ܲ���ָ�ɸ�����Ѫ�ܼ�����������Բ����䡣�ٴ��ϸ�����Ѫ�ܲ��IJ����ݱ���̷�Ϊ��Ѫ����Ѫ�ܲ������Գ�Ѫ������Ĥ��ǻ��Ѫ�ȣ��Լ�ȱѪ����Ѫ�ܲ������������ȱѪ�������Թ���������˨�����Թ�����Ѫ˨�γ����Թ�����ǻ϶���Թ������ȡ���������ָһ����ͻȻ�����ģ������Ի��������Թ����ϰ�Ϊ��ͬ��������Ѫ�ܼ�����
����������Ѫ�ܲ��Ļ����ʸ��ڷ�������Ⱥ�������Գ�Ѫ�Ļ����ʵ��ڷ�������Ⱥ�����Թ����Ļ�����Ϊ��������Ⱥ��4������2001���л�ҽѧ������ѧ�ֻ��ȫ��30ʡ�н�10��סԺ�����߲���֢�ĵ��飬���ϲ���Ѫ�ܲ��߸ߴ�12.2%�������IJ������պ�ǰհ�����в�ѧ�о�����������ȱѪ�������еĶ���Σ�����أ����������Ⱥ��ȣ������������е������ʡ������ʡ������ʽϸߣ�����ָ�����������Ѫ�ܲ��������˻��������������������ҽ�ƾ��ѵ�֧�����Ը��ˡ���ͥ����ᶼ�Ǻܴ�ĸ�����
������һ���ٴ����֡���Ϻͼ������
����1.�Գ�Ѫ�Լ�����������ھ����˶�����ƣ�������������ͻȻ�����硣������ͷʹ�������������Χ������֢״����ʶ�ϰ��ķ����ʽϸߡ�������2��3���ڿ������ȶ���������Լ��أ���Ԥ��ϲ
����2.ȱѪ����Ѫ�ܼ������������峿Ѫ�Ǹߣ�ѪҺŨ���������糿ѪѹҲ����ƫ�ߣ�����ȱѪ����Ѫ�ܲ����������4ʱ��9ʱ֮�䡣
�������������Ͼ��ޣ�����֢״���ᣬ��û�����Ե��Ծ�֢״����֢״��Ϊ��ʱijһ֫�左������������ޣ������½��������ڽ϶̵�ʱ���������Ի��⡣
����������ѹ�����������ߣ���ͷʹ����ػ����ԡ�
����˨�����Թ����ڷ��������ϣ�Ӱ������������Ѫ˨���Թ�����ͬ����������ڽϳ�ʱ�䰲���ٶ��������dz����Դ������������ߣ���ͻȻ��
����3.�����������
�������Գ�Ѫ�Լ�����ȱѪ����Ѫ�ܼ�����������������ͬ���ʼ�����Ϻ���Ҫ�������͵��ٴ�֢״�⣬��Ҫ����Ӱ��ѧ����CT,MRIɨ��ȣ���顣�ڷ���6Сʱ��ɨ���鳣������ȷ�������ʡ�λ�úͷ�Χ��2��3��飬�����˽ⲡ���Ƿ��ȶ����չ��
��������������
����1������֢����ע���������ѭ�����������������ֺ�������ͨ����ֹ����Ѫ֢���������Ʋ������������ߣ����θ�Ⱦ��ע��Ӫ��֧�֡�
����2����ʱ����Ѫѹ������������⣬ӦʹѪѹ������������Χ�ڣ�ͬʱҲӦע���ڽ�Ѫѹ�Ĺ����У���ֹ��Ѫ����
����3�����������ȵ��ؽ���Ѫ�ǡ���Ѫ���½����죬���շ���ѹ���ߺ͵�Ѫ�ǵ�Σ�ա�
����4������Ѫ�ƣ�ʹѪ�Ʊ�����������Χ�ĵ����Է�ֹ��ѹ���ߺ�Ѫ���������շ�Ѫѹ���ߺ�����˥�ߡ�
����5��ע�⼰ʱ���ֺʹ�������Ӧ����ȫ��
����6���Թ�������3��6Сʱ�ڸ���������L-���Էӻ�������Ƽ�������˨���ơ�����ȷ�ų��ڳ�Ѫ����ʹ��������֯������øԭ���������rt-PA����
����7��������ʱ����ʹ�����������ӣ����ء�
����8���Գ�Ѫ���ϴ��ѹ����Ҫ��λʱӦ���Ǽ�ʱ�������ơ�
����9�����翪չ�������ƣ���������1��3���º�ij¾��������У��κ����ƾ�������Ч��
����10����ʱ���ֺʹ�����ѹ���ߡ�
����������Ԥ��
����1�����뾡���ܱ���Ѫ�ǡ�Ѫѹ��Ѫ֬�Ⱥ�ѪҺ����ѧָ�ꡢ��Ѫ���������ȵ������жȺ���Ѫ����Ƥ���ӵȾ���������Χ��
����2���ϸ��ѧ��ѡ��ҩ����������ܽ���Ѫ�ǡ�Ѫѹ��Ѫ֬��ҩ�ﶼ�Ǻ�ҩ�������ܼ���Ѫѹ��Ѫ����������ʹѪѹ�ķ�ȱ�ֵ���͵ij�Чת��ø���Ƽ�������ʹѪ�������Σ���Խ���65%���ϣ���Ѫѹ���ߵĻ��ߣ�С����ʹ��Ҳ��Ч��Ӧ����ѡҩ�һЩ��͡��ҩ�ﲻ�����Խ��͵��̴���Ҳ���Ը���Ѫ������һЩ������Ѫ�����ͣ���Ӱ���ļ���ҩ��������ҩ����б��塢���������ҩ���ٽ������γɵ�˫����ҩ�ﶼӦ���á�
����3����ѪС�����ƣ�ʹ�ð�˾ƥ�ֶԼ��������кͶ�������ȱѪ�����ĸ�������Ч�ģ�����Ϊ����Ԥ����ʩ����˾ƥ��Ҳ����Ϊһ��Ԥ����ʩ���ڴ�Ѫ�ܼ���Σ�յ������ߡ����ʺ�ʹ�ð�˾ƥ�ֵĻ��߿ɷ�������������Ϊ�����
����4���������ʽ��������ʳ�����õ��˶�ϰ�ߣ������������أ���ֹ�������ƣ����̡���Щ��ʩ��Ԥ��������Ѫ�ܼ����л������á�
�����塢�����۲�
������һ�������۲��ı��ֺ�Σ�������������۸���λ���ɳ����������ˣ����Ĥ�쳣����Ĥ����Ѫ�ܣ�������ȣ�����������ۺͰ����ϵĻ����ʸ�����ͬ����������ߡ���������Ĥ������������ʧ������Ҫԭ������������Ĥ���仼�����滼��ʱ��������������������99%��1������60%��2������������20�����ϵĻ��ߣ��������в�ͬ�̶ȵ�����Ĥ���䡣10�����»����Ķ�ͯ���ٷ�������Ĥ���䣬�ഺ�ں���������Ĥ����Σ��������
������������������Ĥ���������������������Ĥ���������۵ı��Ϊ����ֳ�ͣ������ͣ�����ֳ�ͺ������Իư�ˮ�ס�����ֳ����������Ĥ���������ڸı䣬�ַ�Ϊ��ȡ��жȺ��ضȣ���ֳ�Ըı���һ�ֽ�չ�ı䣻�ư�ˮ��������������ͬʱ���ڡ�
��������ֳ����������Ĥ���䣨NPDR���������۵��г�Ѫ����������߽��٣��没���չ����Ѫ������������࣬��Ϊ���NPDR��������ë�ߺ�����Ĥ��Ѫ���쳣ʱ����Ϊ�ж�NPDR����һ����չ�ɼ������������ı䣬����Ĥ�ֲ�ëϸѪ����ע���ۼ�������ޣ���Ϊ�ض�NPDR��
���������Իư�ˮ��Դ������ĤѪ��ͨ���쳣��������ڱ����ͺ���ֳ��֮�䣬����϶������˫Ŀ���۵��ɿ����ư����ֲ�����Ĥ����ˮ������������������Χ��Ӳ���������ư��������ëϸѪ���쳣���������Իư�ˮ�ס����̳��Ļ��ߣ��ư߲��ɳ��ֻư�����ˮ�ס�
������ֳ����������Ĥ���䣨PDR�����۵��ص��dz�������Ĥ����Ѫ�ܵ���ֳ����ά��֯����������Ѫ�ܿ��Է���������Ĥ�κβ�λ��Ҳ���Է����������ϡ�������������Ĥ����Ѫ�ܽ�С���������ά��ֳҲ���٣��������Ѫ����������ά��֯Ҳ���ࣻ�Ժ�����Ѫ���������Ա䣬��άѪ����֯�ز������Ƥ�������ֳ�����������άѪ��Ĥ��ǣ������άѪ��Ĥ�������Լ�����ȫ�IJ���������뵼�²������Ѫ��ǣ��������Ĥ���롣����Ĥ���뷢���ڻư�����ӽ��ư�����ʹ���߳���������Ρ�ǣ��������Ĥ��������������Ĥ�ѿף���������ǣ����Դ���������Ĥ���룬��ɻ���ʧ����
������������۳�����ϲ�ԭ����������⣬��ҪΪ����Ĥ����Ѫ�ܷ�����ëϸѪ����ע����Χ������Ĥ�ܱ߲��������ע���Ĵ��ڣ����º�Ĥ�ͷ�������Ѫ���γɣ�����Ҳ������������Ѫ��������۶�ʧ����
������������������Ĥ���������
����1.����Ŀ��
��������ȵؽ�����������Ĥ���䵼�µ�ʧ�����������ˡ�
����2.���Ʋ���
�����ƶ�����ƻ�������������Ĥ�������ڻ��߳���֢״�����ۻ���ʱ�������ײ��������������ȷ����Ӧ���ۿ�ҽ�����������������Ĥ����������ʱ��ɶ�Ϊһ�꣬��������Ĥ����Ҫ������������
�����۵�����������Ĥ���䣬����ʱ�����14-7��
��14-7 �������ƶ�����ƻ�
|
���������䣨�꣩ |
�״��۵���Ƽ�ʱ�� |
������Ĥ���� ���ڳ�������ʱ�� |
|
0��30 |
ȷ��������� |
ÿ��һ�� |
|
��31 |
ȷ��������� |
ÿ��һ�� |
|
������ |
ȷ������ |
ÿ3����һ�� |
|
�۵�����������Ĥ���䣬������Ĥ����̶��������14-8�� | ||
|
��14-8 ������Ĥ����̶��ƶ�����ƻ� | ||
|
��������Ĥ����̶� |
��������ʱ�� |
|
������Ѫ���Ѫ���� |
ÿ��һ�� |
|
NPDR |
|
|
��� |
ÿ9����һ�� |
|
�ж� |
ÿ6����һ�� |
|
�ض� |
ÿ4����һ�� |
|
�ư�ˮ�� |
ÿ2��4����һ�� |
|
PDR |
ÿ2��3����һ�� |
|
���� |
ÿ��һ�� |
������Ҫ������ֳ����������Ĥ������ٴ�������Ļư�ˮ�ס��о����������ط���ֳ����������Ĥ�������ֳ����������Ĥ������ȫ����Ĥ�������Ա���ͬ���鲻�������Ļ��ߣ�5���ڷ������������½���0.025���Ļ��߿��Լ���50%���ϡ��ٴ�������Ļư�ˮ���ǣ������ڻư����İ�1������ֱ����Χ�ڵ�����Ĥ����Ӳ���������������İ���Χ500��m��Χ��������Ĥˮ�׳��������İ�500��m��Χ���Իư�ˮ�������оֲ��������Ա���ͬ���鲻�������Ļ��ߣ�2���ڷ��������еȳ̶��½��Ļ��߿��Լ���50%���ϡ�
����4.��������Ĥ����IJ�������������
���� Ŀǰ�㷺��չ��������Ӧ֤���������յIJ������Ѫ��ǣ��������Ĥ����Ӱ��ưߡ�ǣ����Դ���������Ĥ���롢��������άѪ����ֳ����ǰ�β�������άѪ����ֳ����ϸ���յ�������ۡ��ư�ǰ���ܵij�Ѫ�ȡ��Բ������Ѫ�ϲ������ϵIJ�����Ӧ���а�����ժ���������г�������������������ֲ���˹����塣
����5.�����ߵİ���������
���� �ܶ��ٴ��о���ʾ��������������������Ĥ�����չ�ӿ죬��˽������������ǰ���۵�����ܿ����ư�ˮ�ס�����NPDR��PDRʱ���Ƚ���ȫ����Ĥ�������ơ��������������أ�����������ڶ���Ӧ����۵ף������ڻư�ˮ�ס�����NPDR��PDRʱ����ȫ����Ĥ�������ơ�
����6.��������Ĥ�����ҩ������
����Ŀǰ��δ֤ʵ��ȷ�е�������������Ĥ�����ҩ�ҩ��������ҪӦΧ������ȫ�����ơ�
����������������
������һ�����������ı��ּ�����
����Mongensen��1����������Ϊ5�ڣ�Լÿ5���չһ�ڣ��÷������ѱ��ٴ�ҽʦ�㷺���á���ʵ��2������������Ҳ������ƣ�ֻ����2����������չ��1�����죨Լÿ3��4���չһ�ڣ����������2����������С������ˣ��������������Ա䣬�Ҷ�ϲ���Ѫѹ����֬Ѫ֢��ء��ֽ���5�ڵ��ٴ��������ּ������£�
����1.��С����˹���
���� ������Ҫ����Ϊ��С���˹��ʣ�GFR�����ߡ������ʱ������Ѫ�ǣ�GFR�仯�Կ���ת�����ڲ��������ɼ���С��ʴ��⣬�����������Բ��䡣
����2.���ٴ����ֵ�������
�������ڿɳ��ּ��������������Ϣʱ�������й�ʣ�UAER��������<20��g/min��<30mg/d����Ӧ��ʱ�����˶������࣬��������ֵ���ڴ����ڻ���GFR���Խϸ���������Ѫѹ�����������ڲ������ɷ��֣�����羵���ȷ������С�����ڲ��䣬��ϵĤ���������������С���Ĥ��GBM���������
����3.��������������
�������ֳ�������������UAER������20��200��g/min��30��300mg/d��Ϊ���ڱ�־�������滯�鵰�������ԡ����ڻ���GFR����������Ѫѹ����ʼ���ߡ����������С�������������С�����Ĥ��GBM����������ԣ�С�����ڳ��ֲ������䡣һ����Ϊ�Ӵ��������ಡ���Ѳ����档
����4.�ٴ�����������
�����滯�鵰�����Լ���־������ڣ����ڲ����չѸ�٣��������ڳ��ִ���������>3.5g/d���������ۺ��������������ۺ������������ִ�����ˮ����ǻ��Һ������������Ч����ڻ���GFR���ͣ�Ѫѹ�������ߡ����������С����أ�������С����Ӳ�����Ұ������������С��ή������������ά����
����5.��˥����
�����ӳ��ִ���������ʼ�����������ܼ��ٶ�ֱ����˥�ߡ����߳�������ƶѪ���������������ԭ������С����һ�����������ѽ�����˥���ڣ���������ȴ�������ɳ��������ۺ������⽫������������������������������Ƶ����ѣ���Ϊ���߸���ά��Ӫ�������׳��ֲ���֢����ʱ����������飬��ֻ�ܼ����������ಡ�䣬��������С��Ӳ�����ķϣ���������С��ή���������ʹ㷺��ά����
����Ϊ�ˣ����������ɲο����±�������ϣ�����ʷ������6��10�����ϣ������ֳ�������������UAER��20��200��g/min��30��300mg/d������Ӧ������������������������ʷ�����������ԣ��������ִ��������������ۺ�������Ӧ���ǣ����ٴ�������������ϡ�������ȷ����������ǰ��������������༲������Ҫʱ���������̲�����顣��֯������������С��������ϸ����������ϵĤ��������������GBM�㷺���������迿�羵���֤ʵ�����������Kimmelstiel-Wilson���ʱ����ϼ�ȷ���������������۵ײ����Ϊ����Ѫ�ܲ���֢�����߳�ͬʱ���֣���˷��������۵ײ��䣨������Ѫ�����ȣ������ṩ֧������������ϵ���֤��
����������Ԥ�����������Ĵ�ʩ
�����������߲����������ƴ�ʩ��Ԥ�����������ķ�������չ
����1.���Ƹ�Ѫ��
�����ӻ�������Ӧ�������Ƹ�Ѫ�ǣ�����һ��Ҫ�ϸ��꣺�ո�Ѫ��<6.1mmol/L��110mg/dl�����ͺ�Ѫ��<8.0mmol/L��144mg/dl�����ǻ�Ѫ�쵰��<6.5%�����ܴ�꽫����ЧԤ�����������ķ�������չ�����Ƹ�Ѫ�ǵľ����ʩ��μ���ָ���й����ݡ�
����2Ӧ��Ѫ�ܽ�����ת��ø���Ƽ���ACEI����Ѫ�ܽ�����II�������ͼ���ARB��
���������ߴӳ���������������������Ѫѹ��Ӧ����ACEI��ARB����Ϊ����ҩ�����ܽ���Ѫѹ�����һ��ܼ���������ӻ�����չ��
����������ҩʱ��ע�⣺1������ѡ�ó�Ч��˫ͨ�����������⣩��й�
����2����ҩ���С����ʼ��������ʱ������Ϊ��Ч����������ӻ�����չ����ϴ�ҩ�����Ƚ�Ѫѹ��������ҩʱ��Ҫ�ã��������꣩��3��Ҫ���й۲츱��������ԡ���Ѫ�ؼ�Ѫ�弡��Ѹ�����ߣ����ڷ�ҩǰ30%��50%������������ȱѪʱ���ȣ���Ҫʱͣҩ�����Ǹ�Ѫ�ر���������ȱѪ������Ҽ����ظ�ԭ��ˮƽ���Կ�������ҩ��4��˫����������խ�����PѪ�弡��>265��mol/L��3mg/dl���Ļ��߲����ô���ҩ�
����3.���Ƹ�Ѫѹ
�������Ǻϲ���Ѫѹ�������߶�Ҫ�������Ƹ�Ѫѹ������ҲҪ�ϸ��ꣻ��������<1.0g/d�Ļ��ߣ�ѪѹӦ���ƴ�<130/80mmHg����>1.0g/d�Ļ��ߣ�ѪѹӦ���ƴ�<125/75mmHg�����Ƹ�Ѫѹ�ľ����ʩ��μ���ָ���й����ݡ�
����4.���Ƹ�Ѫ֬
�������Dz�����֬Ѫ֢�������߶�Ӧ���е�֬���ƣ��Խ�Ѫ֬���ƴ�꣺TC<4.5mmol/L,LDL-C<2.6mmol/L,HDL-C>1.1mmol/L,TG<1.5mmol/L.�Ա��������ٶ��ԣ�����TC��LDL-C��Ϊ��Ҫ�����Ƹ�֬Ѫ֢�ľ������ƴ�ʩ��μ���ָ���й����ݡ�
������������������������
����1.�������ۺ���������
���������������������ۺ���ֻ�ܶ�֢���ƣ����������ף����������ѡ������Ⱦ�����ע����Һ���ݣ��پ���ע���������������������ȣ����ܻ�Ч��Ӧ�þ�������ҺʱҪע�⣺
����1������ѡ�ͷ�������������������20��40kD�������һ����۴�Ѫ����706��Ѫ����������25��45kD�����˷������Ľ������ʼ�����������������������ˡ�
����2��Ҫ�ú������Ƕ������Ȼ��ƵĽ���Һ���������ˮ��������������ʱ����������ȵ�������ƿ�������������ǡ�
����3������������400ml/dʱ��Ҫ���û�����������Һ��������������������⣬���߱����ϸ���õ�����ʳ��ʳ��3g/d����
�����������ˮ����ǻ��Һ��������������Чʱ��������ѪҺ�����������г�����ˮ�������ߴ���Ѫ�������㣬����ǰ���������佺��Һ�������ƺó����ٶȼ���ˮ�����Ա��ⷢ����Ѫѹ��
����2.�������ܲ�ȫ������
���������������߳��������ܲ�ȫʱӦ��ȡ�����ۺ����ƣ�
������1���ӻ�����չ��������Ӧ��ǰ����ʩ����ACEI��ARB�����Ƹ�Ѫ�ǡ���Ѫѹ����Ѫ֬���⣬��Ӧ���Ƶ������������������������ܲ�ȫ���ߵ���������Ӧ���Ƶ�ʲô�̶ȣ���ʶ��δͳһ���ɲο��ķ����ǣ�ÿ�ս�ʳ������0.6g/kg��ͬʱ���æ�ͪ��-�������Ƽ�������֤ÿ��������125��146kJ/kg��30��35kcal/kg���Ա���Ӫ�������ķ����������м���Ӫ��ָ�꣩��
������2���ų����ڴ�л������ó�θ�����ƣ������ú���ҩ��Ƶ�ҩ����ú���Ƶ���ҩ��������೦��
������3��ά�ֻ����ڻ���ƽ�⣺Ӧע�����ˮ������ʼ����ƽ�����ң�Ӧʹ�ú�ϸ�������ؼ�������������ƶѪ����ʹ�û���ά����D3���Ƽ�״���ٹ��ܿ�����������ԹDz���
������4������ĩ��˥�ߵ�:���ƣ�ͬ�������ಡ������ĩ��˥��һ����ֻ�ܽ�������������ư���ѪҺ������Ĥ��������ֲ�����ǣ�������������ĩ��˥���߿�ʼ��Ҫ�磬��Ϊ�����̷������ġ���Ѫ�ܼ����䣬��������Ӱ�컼�����������������ʡ�����������ʼ����ָ���ǣ�Ѫ�弡��>530��mol/L��6mg/dl��,���������<15��20ml/min��
�������ģ������ܲ�ȫʱ��������
���������ܲ�ȫ������Ӧ����������ҩ����һЩ����Ҫ������ӡ�
����1.�ȵ���
���������ܲ�ȫ����������ȵ�����������ʱ�����ȵ��ؿ��ܴ������ֽ�Ȼ��ͬ������������ܲ�ȫʱ��С�����ƻ��������ȵ��ؽ�����٣��ȵ������������һ���棬�����ܲ�ȫ�����ֿ��ܲ����ȵ��صֿ�����ʱ��Ӵ��ȵ��ؼ���������Ч����Ѫ�ǡ���ͬ���������ͬ��Ӧ���м���Ѫ�DZ仯�����ڼ�����
����2.�ڷ�����ҩ
���������ܲ�ȫ������ijЩ�ڷ�����ҩ���ڴ�л�����仯��������ڼ�����ͣ�á�
����1��������ҩ������ҩ��Ҫ������й�������ܲ�ȫʱ����ҩ��������շ���Ѫ�ǣ���Ӧ���á����������ͪ���⣬���л�����5%������й�����ᵽ�ж������ܲ�ȫʱ�Կ�Ӧ�ã�����ĩ��˥�������ʵ�������
����2����������ҩ������ҩ���ᡢ�ж������ܲ�ȫʱ�Կ�Ӧ�á�
����3��˫����ҩ������ҩ��Ҫ������й�������ܲ�ȫʱ����ҩ����������������������ж�����Ӧ���á�
����4���������ͪ��ҩ������ҩ���ᡢ�ж������ܲ�ȫʱ�Կ�Ӧ�á�
����5��������ø���Ƽ�������ҩ�ڷ����Լ2%������Ѫ��������ӳ����ų����������ܲ�ȫʱ�Կɷ��á�

